Grippe saisonnière
La grippe saisonnière est très contagieuse. Chez l’être humain, elle est causée par les virus influenza A et influenza B
Dernière mise à jour le 06 mars 2026
L’essentiel
- La grippe saisonnière est une infection respiratoire aiguë
- La majorité des cas sont bénins
- Elle est cependant associée à une morbidité et une mortalité significatives chez des personnes à risque de complications ou qui présentent d’autres pathologies
Origine de la grippe
Historique
La grippe serait apparue chez les oiseaux il y a six mille ans. Elle serait parvenue jusqu’à l’homme au néolithique, il y a 4 500 ans, avec le développement de la domestication des animaux.1
La première mention de la maladie daterait du Ve siècle avant notre ère. Quant à lui, le mot « influenza » serait apparu au XVe siècle à Florence, dans l’expression influenza di freddo (sous l’influence du froid), l’épidémie survenant lors des refroidissements saisonniers.1
Le caractère saisonnier de la maladie est bien connu. Jusqu’au XVIIIe siècle, les épidémies sont régionales. L’apparition de pandémies, environ trois fois par siècle, est sans doute le résultat du développement de l’agriculture et de l’accélération des déplacements.1
En 1889 apparait la « grippe russe » qui, d’abord circonscrite dans la partie centrale de la Russie, finit par atteindre l’Europe, les pays méditerranéens, les Amériques du nord et du sud, avec un lourd bilan d’un million de morts, dont 150 000 en Europe.1 C’est au XIXe siècle qu’une bactérie est faussement désignée comme agent pathogène de la grippe ; elle sera appelée bacillus influenza (aussi connu sous le nom de bacille de Pfeiffer).1
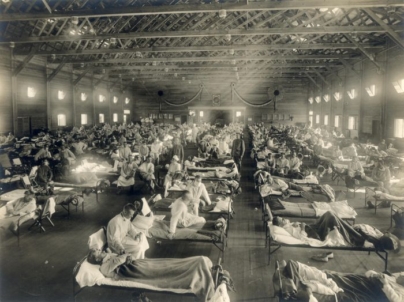
En 1918, en pleine guerre mondiale, des soldats américains infectés aux Etats-Unis répandent la grippe à l’Europe entière. Elle sera dénommée « grippe espagnole », l’Espagne étant le seul pays à publier librement les informations relatives à cette épidémie.1 Entre 1918 et 1919, la pandémie tue entre 21 et 73 millions de personnes dans le monde.1 En 1918, René Dujarric de la Rivière filtre le virus de la grippe. La première souche humaine du virus, la souche H1N1 (celle responsable de la grippe espagnole), ne pourra cependant être isolée qu’en 1933.1
Épidémiologie récente en France
Selon Santé Publique France, il y a eu en France métropolitaine pour la saison 2024-25, plus de 3 millions de consultations en médecine de ville, plus de 29 000 hospitalisations et environ 9 000 décès liés à la grippe, concentrés sur une durée moyenne de dix semaines d’épidémie, et ce avec des variations importantes d’une épidémie à l’autre et selon l’âge.2,3
Le virus de la grippe
Les virus grippaux sont des virus enveloppés à ARN. Ils appartiennent à la famille des Orthomyxoviridae. Trois types de virus influenza affectent l’être humain : influenza A, B et C.4,5
Le type influenza A est divisé en sous-types sérologiques, selon la nature des deux glycoprotéines de surface hémagglutinine (HA) et neuraminidase (NA).4,5 Les virus grippaux B sont subdivisés en deux lignées : la lignée B/Yamagata ou la lignée B/Victoria.4
Les virus grippaux A et B circulent et provoquent des épidémies saisonnières, le virus influenza A étant également responsable de pandémies.4 Plus précisément, la grippe saisonnière humaine est causée par les virus influenza A(H1N1)pdm09*, A(H3N2) et influenza B (Victoria/Yamagata).4
* depuis qu’il a causé la pandémie de 2009, le virus A(H1N1) s’écrit sous la forme A(H1N1)pdm09. Il a remplacé le précédent virus A(H1N1) qui circulait avant cette date4
Les problèmes les plus complexes de l’épidémiologie de la grippe sont liés à la variabilité du virus influenza. Les virus variant au cours du temps, l’organisme n’est pas capable de les reconnaître et donc de se défendre.5
Transmission
La grippe saisonnière est très contagieuse. La transmission entre individus se fait surtout par les aérosols à grosses particules émis lors des éternuments ou de la toux lorsque les personnes sont à proximité.4,5 Les gouttelettes infectieuses ne restent pas en suspension dans l’air ; elles sédimentent sur les surfaces et les objets, créant une autre source possible de transmission.5 Le virus peut également se propager par des mains contaminées.4
Dans les climats tempérés, les épidémies saisonnières se produisent principalement en hiver. Dans les régions tropicales, les épidémies sont plus irrégulières, la grippe pouvant se manifester tout au long de l’année.4
Diagnostic
La durée moyenne d’incubation est d’environ deux jours, comprise entre un et quatre jours.4,5
Deux méthodes biologiques sont à disposition :
- La RT-qPCR (PCR quantitative après transcription inverse), considérée comme la méthode de référence, a une sensibilité généralement > 95 % selon les plateformes et la qualité du prélèvement
- Les tests antigéniques rapides, dont la sensibilité est plus variable (environ 50–80 %) mais avec une spécificité élevée, permettant un diagnostic rapide en pratique clinique
Les prélèvements recommandés sont nasopharyngés ou oro-pharyngés. Ils doivent être réalisés idéalement dans les trois à cinq jours suivant le début des symptômes, correspondant à la période de réplication virale maximale dans les voies respiratoires supérieures.
Symptômes et traitement de la grippe saisonnière
Les symptômes
La grippe est caractérisée par une atteinte systémique aiguë. Les symptômes associés sont une fièvre d’apparition brutale, des céphalées, des douleurs musculaires, une toux sèche, des maux de gorge et un écoulement nasal.4,5
La majorité des cas sont bénins, mais la grippe est associée à une morbidité et une mortalité significatives. Les taux de létalité augmentent fortement chez les plus de 65 ans, les enfants de moins de 5 ans, les femmes enceintes et les patients atteints de pathologies chroniques (cardio-respiratoires, métaboliques, immunodépression).4
Les traitements
La grippe non compliquée se résout spontanément en trois à sept jours.4,5
Pour les personnes qui présentent des symptômes graves, qui sont à risque de complications ou qui présentent d’autres pathologies, divers traitements sont disponibles :
- L’oseltamivir et le zanamivir, des inhibiteurs de la neuraminidase, sont indiqués chez les patients à risque de complications (personnes âgées, enfants très jeunes, femmes enceintes, immunodéprimés, patients avec maladies chroniques) ou en cas de forme grave nécessitant une hospitalisation. L’efficacité est maximale si le traitement est initié dans les 48 premières heures après l’apparition des symptômes. L’oseltamivir est administré par voie orale pendant cinq jours, tandis que le zanamivir se prend par inhalation, avec des restrictions pour les patients souffrant de maladies respiratoires sévères6
- Le baloxavir marboxil, un inhibiteur de l’endonucléase, présente l’avantage d’une dose unique, ce qui facilite l’observance. Il a été approuvé en tant que traitement de la grippe pour les patients à risque de complications dans plus de 74 pays à travers le monde et commercialisé dans 33 pays, dont cinq en Europe.7 Son efficacité est maximale lorsqu’il est administré tôt, idéalement dans les 48 heures suivant le début des symptômes.8 L’essai clinique randomisé CENTERSTONE a également montré qu’il s’agissait d’une option thérapeutique à considérer en post-exposition, le risque de transmission étant significativement réduit de 29 % par rapport au groupe placebo9
- Les antiviraux peuvent être utilisés en prévention post-exposition dans les 48h après le premier contact avec une personne infectée pour protéger les personnes à haut risque10
Les pistes de recherche
Des recherches sont en cours pour développer de nouvelles thérapies adaptées aux nouveaux variants émergents, notamment avec des études précliniques et cliniques qui explorent l’efficacité des anticorps monoclonaux et polyclonaux, et d’autres molécules antivirales.11
- Anticorps monoclonaux
 Certains anticorps monoclonaux, TCN-032 de Theraclone, VIS410 de Visterra, CR6261 et CT-P27 de Celltrion,12-15 ont montré lors d’essais cliniques de phase II une bonne tolérance avec des bénéfices sur la réduction de la symptomatologie et de la charge virale pour la grippe. De nombreux autres candidats sont en développement, sans encore avoir démontré une efficacité significative. Parmi ceux-ci, VIR-2482 (Vir Biotechnology) et MHAA4549A (Genentech), tous les deux étudiés dans des essais cliniques de phase II.16,17
Certains anticorps monoclonaux, TCN-032 de Theraclone, VIS410 de Visterra, CR6261 et CT-P27 de Celltrion,12-15 ont montré lors d’essais cliniques de phase II une bonne tolérance avec des bénéfices sur la réduction de la symptomatologie et de la charge virale pour la grippe. De nombreux autres candidats sont en développement, sans encore avoir démontré une efficacité significative. Parmi ceux-ci, VIR-2482 (Vir Biotechnology) et MHAA4549A (Genentech), tous les deux étudiés dans des essais cliniques de phase II.16,17
- Anticorps polyclonaux
Plusieurs études avaient suggéré que l’utilisation thérapeutique de plasma de convalescents remis d’une grippe saisonnière pouvait être bénéfique chez des personnes atteintes d’une grippe A sévère. Une étude de phase III a montré qu’il n’en était rien.11
- Immunoglobulines
FLU-IGIV, une immunoglobuline dérivée du plasma humain, a été testée contre H1N1pdm09 dans des modèles murins et de furets. FLU-IGIV a réussi à protéger les souris (taux de survie de 100 %) contre une dose virale mortelle ; le taux de survie observé de 60 % était supérieur à celui observé avec l’oseltamivir.18 Une étude de phase II est en cours chez des adultes hospitalisés pour évaluer son efficacité dans le traitement d’une grippe sévère.19
Une autre immunoglobuline, SAB-176, fait l’objet d’un essai clinique de phase II afin d’évaluer sa sécurité et son efficacité thérapeutique contre H1N1 chez des participants adultes en bonne santé.20
La prévention
Les vaccins
 La vaccination antigrippale constitue le principal moyen de prévention de la grippe saisonnière en France. Elle repose sur l’administration annuelle de vaccins inactivés, en raison de la variabilité antigénique des virus influenza et de la nécessité d’adapter la composition vaccinale chaque saison.21
La vaccination antigrippale constitue le principal moyen de prévention de la grippe saisonnière en France. Elle repose sur l’administration annuelle de vaccins inactivés, en raison de la variabilité antigénique des virus influenza et de la nécessité d’adapter la composition vaccinale chaque saison.21
L’objectif de couverture vaccinale chez les personnes âgées de 65 ans et plus, les personnes atteintes de maladies chroniques, les femmes enceintes, les personnes immunodéprimées ainsi que les professionnels de santé a été fixé à 75 % en 2009 par l’OMS.22
En 2024-2025, la couverture vaccinale était estimée à 54 % chez les 65 ans et plus, et 25 % chez les moins de 65 ans à risque, des valeurs relativement stables en comparaison de celles de 2023-2024.2 Chez les moins de de 18 ans à risque, elle était de 13 % en 2024-2025.23
Les vaccins utilisés en France pour la saison 2025-2026
Les vaccins antigrippaux utilisés en France sont majoritairement trivalents, contenant deux souches de virus influenza A (A(H1N1)pdm09 et A(H3N2)) et une souche de virus influenza B (lignée Victoria), conformément aux recommandations émises par l’OMS pour l’hémisphère Nord*.24,25
Plusieurs vaccins sont recommandés par l’EMA, parmi lesquels les vaccins standard Vaxigrip®, Influvac®et Flucelvax® administrables à toute la population éligible, y compris aux enfants de 2 à 17 ans sans comorbidités.23 Des vaccins spécifiquement destinés aux personnes âgées de 65 ans et plus sont également disponibles, le vaccin à dose élevée Efluelda® et le vaccin adjuvanté Fluad®.26 Ces formulations renforcées visent à améliorer la réponse immunitaire chez les sujets âgés en lien avec l’immunosénescence. D’après la plus grande étude d’efficacité en vie réelle d’un vaccin antigrippale inactivé à haute dose jamais réalisée, FLUNITY-HD, incluant près d’un demi-million de participants, le vaccin Efluelda/Fluzone High-Dose de Sanofi offre une protection supérieure à la fois contre l’infection grippale et les hospitalisations par rapport aux vaccins à dose standard chez les adultes de 65 ans et plus.27
* la souche grippale de la lignée B/Yamagata n’a pas été détectée depuis mars 2020
En France, la vaccination antigrippale est recommandée chaque année chez les personnes âgées de 65 ans et plus, les personnes atteintes de maladies chroniques, les femmes enceintes, les personnes immunodéprimées ainsi que les professionnels de santé.
Les pistes de recherche
La dernière édition du guide « Preferred product characteristics for next generation influenza vaccines » de l’OMS préconise la mise au point de vaccins antigrippaux améliorés, novateurs et universels. Elle souligne également la nécessité de disposer de vaccins offrant une protection plus large et plus longue, une plus grande efficacité contre les formes graves de la maladie et un délai de production réduit pour une vaccination annuelle.28 Actuellement, plus de 50 candidats vaccins issus de plateformes différentes sont en phase préclinique ou clinique.
- Vaccins à ARNm
Trois candidats de nouvelle génération sont actuellement en phase III : le vaccin quadrivalent modRNA de Pfizer, le mRNA-1010/1083 de Moderna et le NanoFlu de Novavax et Emergent BioSolutions. Les deux candidats développés par Pfizer et Moderna utilisent une plateforme ARNm combinée contre le SARS-CoV-2/la grippe et le virus respiratoire syncytial (VRS)/la grippe. Les derniers résultats de l’essai de phase III mené sur le vaccin mRNA-1010 à dose unique de Moderna démontrent des taux de séroconversion plus élevés pour les souches virales A et B que le vaccin de référence à dose standard homologué.29 Moderna teste également un vaccin à ARNm triple contre le SARS-CoV-2/la grippe/le VRS. Trois de ces produits combinés sont actuellement étudiés en phase II.
- Vaccins universels contre Influenza A
Les vaccins antigrippaux à large spectre protègent contre plusieurs virus grippaux, mais ne répondent pas aux critères d’un vaccin universel*.
Bien qu’aucun des vaccins universels ou à large spectre ne soit actuellement étudié dans un essai clinique de phase III, les résultats obtenus au stade précoce de développement sont prometteurs.
L’un d’eux est le candidat OVX836 (Osivax), une protéine recombinante comprenant la nucléoprotéine du virus de la grippe H1N1. Son immunogénicité et sa sécurité ont été évaluées dans une étude clinique de phase II chez des sujets sains âgés de 18 à 55 ans et chez des personnes âgées de 65 ans et plus. L’étude a confirmé que OVX836 est un candidat vaccin sûr et bien toléré, qui suscite des réponses immunitaires humorales et cellulaires (lymphocytes T) chez les jeunes adultes comme chez les personnes âgées.30
D’autres candidats, faisant tous l’objet d’étude clinique en phase II, sont prometteurs comme le MVA-NP+M1 de Barinthus Biotherapeutics,31 le BPL-1357 de NIAID32 et le FLU-v de PepTcell Limited.33
- Vaccins intranasaux et combinés
H3N2 M2SR de FluGen est un vaccin à virus vivant à réplication unique. Il est le seul candidat à avoir été testé chez les enfants de 9 à 17 ans dans un essai de phase I.34 Il a conduit à une réduction significative de l’infection et des symptômes grippaux et à une induction des réponses immunitaires contre les souches dérivées dans une essai clinique de phase II.35
- Vaccins à virus inactivé avec adjuvant
Des vaccins à virus entier inactivé sont en cours d’évaluation pour leur capacité à induire une réponse immunitaire forte. Un essai clinique de phase III a montré qu’un vaccin contre la grippe formulé avec l’adjuvant MF59 provoquait une réponse immunitaire spécifique à l’antigène plus importante et prolongée que les vaccins sans adjuvant.36
Un vaccin antigrippal saisonnier adjuvanté à base d’adénovirus vecteur H1N1 et d’hémagglutinine, le VXA-A1.1 de Vaxart, est actuellement étudié dans une étude de phase II sur des volontaires adultes en bonne santé.37
* La protection peut être spécifique à un sous-type (comme le H1 seul), à un multi-sous-type au sein d’un même groupe, pan-groupe (tout le groupe 1 ou tout le groupe 2 de la grippe A) ou peut concerner tous les virus de la grippe B
Les actions de recherche de l’ANRS Maladies infectieuses émergentes sur la grippe saisonnière
Les projets de recherche
L’ANRS MIE soutient de nombreux projets portant sur les virus responsables de l’influenza/grippe, y compris sur les sous-types H3N2 et H1N1 :
- VIRIPATH: Infectivité Virale et la Physique de la Transmission Aéroportée entre Hôtes
- I2R-VRI: Réponses immunitaires innées dans les infections respiratoires virales
- PREDA-VIR: Une approche pour prédire et contrer le potentiel d’adaptation de virus zoonotiques de la grippe A à l’homme sur la base des compatibilités entre protéomes viral et humain
- MREID: Observer la résilience aux maladies infectieuses émergentes
- MCARE-Bats: Mécanismes moléculaires et cellulaires des réponses antivirales chez les chauves-souris : une perspective évolutive et fonctionnelle
- UNFIRE: Accélérer notre capacité à comprendre et combattre l’immuno-pathologie causée par les infections respiratoires dues à des virus émergents : des modèles de souris aux patients en passant par les macaques
- TRAVERSE: Voies de transmission des virus respiratoires
- CATMOS: Balise de surveillance continue des menaces biologiques aéroportées
- DISORDER-TO-ADAPT: Désordre intrinsèque des protéines et adaptation des virus de la grippe A à l’espèce hôte
- VIR-HOST-PREDICT: Prédiction précoce des complications des infections virales respiratoires chez les patients immunodéprimés
- VIR-IFN: Défauts génétiques et autoanticorps altérant l’immunité médiée par les interférons chez les patients avec infections virales émergentes
- IRAFRICA: Épidémiologie des infections respiratoires aiguës virales en Afrique sub-saharienne
- CHAZEP-SEA: Co-développement d’approches sensibles au patrimoine pour la prévention de l’émergence de zoonoses en Asie du Sud-Est
- ViRespiME: Épidémiologie des viroses respiratoires (SARS-CoV-2, virus respiratoire syncytial, et influenza) chez les femmes enceintes et leurs nourrissons en Afrique de l’Ouest pour orienter les stratégies vaccinales
- OptIViRes: Optimisation du parcours de soins des patients atteints de viroses respiratoires par le phénotypage interféron nasopharyngé en soins primaires
- RESPIVAC : Efficacité en population de la vaccination pour la prévention des infections respiratoires virales chez l’adulte hospitalisé
Animations scientifiques
AvATher est un groupe d’experts consultatif de l’ANRS MIE qui fournit des avis fondés sur des données probantes concernant des molécules antivirales et anticorps monoclonaux en phase finale de développement préclinique ou en phase clinique. Ces molécules et anticorps ciblent la Covid-19, mais également d’autres viroses respiratoires comme la grippe.
Plusieurs actions coordonnées (AC) ont comme périmètre d’action les virus de la grippe saisonnière dans des champs disciplinaires différents. C’est le cas de l’AC Viroses Respiratoires, de l’AC Vaccin Viroses Respiratoires et de l’AC Transmission interhumaine des virus respiratoires.
Cellules Emergence
Depuis 2023, l’ANRS MIE dispose d’une cellule émergence de niveau 1 pour la grippe aviaire A(H5N1), ainsi qu’un groupe de travail multi-institutionnel sur la situation des virus influenza aviaires hautement pathogènes (IAHP) H5N1.
En raison de la circulation très active et de plus en plus précoce des sous-type H1N1 et H3N2 responsables de la grippe saisonnière humaine en France et en Europe depuis 2 ans, une cellule émergence de niveau 1 a été créée. Elle a récemment fusionné avec celle de l’H5N1.
Par ailleurs, une réunion de recherche s’est tenue le vendredi 23 janvier 2026 avec pour objectif de faire un point sur la situation épidémiologique, virologique et clinique, et pour discuter des priorités de recherche.
À l’issue de cette réunion, qui a réuni plus de 53 participants multidisciplinaires et multi-institutionnels, les grandes questions de recherche suivantes ont été discutées :
- Dynamiques épidémiologiques et déterminants de la sévérité
- Quels sont les facteurs expliquant le démarrage précoce et l’intensité élevée de la saison grippale 2025-2026 en France et en Europe ?
- Pourquoi observe-t-on une atteinte particulièrement marquée chez les enfants de moins de cinq ans durant cette saison ?
- Évolution virologique, échappement antigénique et surveillance
- Dans quelle mesure l’évolution rapide du H3N2 (variant K) entraîne-t-elle un échappement antigénique vis-à-vis des vaccins de l’hémisphère nord ?
- Quels sont les mécanismes virologiques expliquant la meilleure reconnaissance du variant K par les sérums vaccinaux de l’hémisphère sud ?
- Quelle est la valeur prédictive des modèles animaux, notamment le furet,* pour évaluer l’impact réel de ces évolutions virologiques chez l’humain ?
- Impact clinique et phénotypes de gravité
- Quels profils cliniques ou biologiques précoces permettent de prédire l’évolution vers des défaillances d’organes ou une forme sévère de l’infection ?
- Contre-mesures thérapeutiques et résistances antivirales
- Quels sont la prévalence et l’impact clinique de la résistance à l’oseltamivir chez les patients hospitalisés ou en réanimation, notamment en cas d’infection par H1N1 ?
- Stratégies de vaccination
- Quels leviers permettraient d’augmenter la couverture vaccinale, en particulier chez les enfants et les populations à risque ?
*Le furet est modèle animal de prédilection pour étudier l’infection par le virus de la grippe. Il reproduit de manière fidèle l’évolution de la maladie chez l’être humain, avec les mêmes symptômes, et réponse immunitaire. Cependant, année après année, ce modèle semble être moins adapté en raison des souches humaines récentes, surtout H3N2, qui ont évolué pour s’adapter très finement à l’hôte humain. Ceci peut donc engendrer une moins bonne infection chez le furet, une moins bonne réplication dans les voies respiratoires, et donc une maladie atténuée. Un vaccin peut ainsi sembler peu efficace chez le furet alors qu’il pourrait l’être chez l’humain et inversement38
Références
- Lumni enseignement : Virus de la grippe : 2 000 ans de traque scientifique. https://enseignants.lumni.fr/parcours/1428/virus-de-la-grippe-2000-ans-de-traque-scientifique.html (consulté le 19/02/2026)
- SpF : Infections respiratoires aiguës (grippe, bronchiolite, COVID-19). Bilan de la saison 2024-2025 https://www.santepubliquefrance.fr/maladies-et-traumatismes/maladies-et-infections-respiratoires/grippe/documents/bulletin-national/infections-respiratoires-aigues-grippe-bronchiolite-covid-19-.-bilan-de-la-saison-2024-2025 (consulté le 19/02/2026)
- SpF : Prévisions de la grippe saisonnière en France : un outil supplémentaire pour anticiper l’évolution de l’épidémie. https://www.santepubliquefrance.fr/presse/2025/previsions-de-la-grippe-saisonniere-en-france-un-outil-supplementaire-pour-anticiper-l-evolution-de-l-epidemie (consulté le 19/02/2026)
- OMS : Grippe saisonnière. https://www.who.int/fr/news-room/fact-sheets/detail/influenza-(seasonal) (consulté le 19/02/2026)
- Vabret A, et al. La grippe saisonnière. Pathologie Biologie 2010 ; 58 :e51-e57
- Jefferson T, et al. Neuraminidase inhibitors for preventing and treating influenza in adults and children. Cochrane Database Syst Rev 2014;2014(4):CD008965
- ema : Résumé des caractéristiques du produit – Xofluza : https://www.ema.europa.eu/fr/documents/product-information/xofluza-epar-product-information_fr.pdf (consulté le 03/03/2026)
- Hayden FG, et al. Baloxavir marboxil for uncomplicated influenza in adults and adolescents. N Engl J Med 2018;379(10):913-923
- Monto AS, et al. Efficacy of baloxavir treatment in preventing transmission of influenza. N Engl J Med 2025;392(16):1582-1593
- Gaitonde DY, et al. Influenza: Diagnosis and treatment. Am Fam Physician 2019;100(12):751-758
- Beigel JH, OldachD. Polyclonal and monoclonal antibodies for the treatment and prevention of influenza. J Infect Dis 2025;232(Supplement3):S347-S358
- Ramos EL, et al. Efficacy and safety of treatment with an anti-m2e monoclonal antibody in experimental human influenza. J Infect Dis 2015;211(7):1038-1044
- Hershberger E, et al. Safety and efficacy of monoclonal antibody VIS410 in adults with uncomplicated influenza A infection: Results from a randomized, double-blind, phase-2, placebo-controlled study. EBioMedicine 2019:40:574-582
- Han A, et al. Safety and efficacy of CR6261 in an influenza A H1N1 healthy human challenge model. Clin Infect Dis 2021;73(11):e4260-e4268
- gov : https://clinicaltrials.gov/study/NCT03511066 (consulté le 03/03/2026)
- gov : https://clinicaltrials.gov/study/NCT05567783 (consulté le 03/03/2026)
- gov : https://clinicaltrials.gov/study/NCT02623322?term=MHAA4549A&rank=4&tab=study (consulté le 03/03/2026)
- Qiu H, et al. Efficacy of anti-influenza immunoglobulin (FLU-IGIV) in ferrets and mice infected with 2009 pandemic influenza virus. Antiviral Res 2020:180:104753
- gov : https://clinicaltrials.gov/study/NCT03315104 (consulté le 03/03/2026)
- gov : https://clinicaltrials.gov/study/NCT04850898 (consulté le 03/03/2026)
- WHO: Global influenza programme – Vaccines https://www.who.int/teams/global-influenza-programme/vaccines (consulté le 03/03/2026)
- WHO: Influenza vaccination coverage and effectiveness https://www.who.int/europe/news-room/fact-sheets/item/influenza-vaccination-coverage-and-effectiveness (consulté le 03/03/2026)
- ameli : Grippe 2025-2026 : renforcer la vaccination des enfants à risque https://www.ameli.fr/pharmacien/actualites/grippe-2025-2026-renforcer-la-vaccination-des-enfants-risque (consulté le 03/03/2026)
- WHO: Recommended composition of influenza virus vaccines for use in the 2025-2026 northern hemisphere influenza season https://www.who.int/publications/m/item/recommended-composition-of-influenza-virus-vaccines-for-use-in-the-2025-2026-nh-influenza-season (consulté le 03/03/2026)
- HAS : Transition du vaccin antigrippal FLUENZ, de sa forme quadrivalente à une forme trivalente, dans la stratégie de vaccination contre la grippe saisonnière https://www.has-sante.fr/jcms/p_3574072/en/transition-du-vaccin-antigrippal-fluenz-de-sa-forme-quadrivalente-a-une-forme-trivalente-dans-la-strategie-de-vaccination-contre-la-grippe-saisonniere (consulté le 03/03/2026)
- HAS : Vaccination contre la grippe saisonnière des personnes de 65 ans et plus. Place des vaccins Efluelda et Fluad https://www.has-sante.fr/jcms/p_3604446/fr/vaccination-contre-la-grippe-saisonniere-des-personnes-de-65-ans-et-plus-place-des-vaccins-efluelda-et-fluad (consulté le 03/03/2026)
- Johansen ND, et al. Effectiveness of high-dose influenza vaccine against hospitalisations in older adults (FLUNITY-HD): an individual-level pooled analysis. Lancet 2025;406(10518):2425-2434
- WHO: WHO preferred product characteristics for next generation influenza vaccines, second edition https://www.who.int/publications/i/item/9789240114982 (consulté le 03/03/2026)
- Han A, et al. Safety and efficacy of CR6261 in an influenza A H1N1 healthy human challenge model. Clin Infect Dis 2021;73(11):e4260-e4268
- Jacobs B, et al. Evaluation of safety, immunogenicity and cross-reactive immunity of OVX836, a nucleoprotein-based universal influenza vaccine, in older adults. Vaccines (Basel) 2024;12(12):1391.
- Evans T, et al. Assessment of CD8+ T-cell mediated immunity in an influenza A(H3N2) human challenge model in Belgium: a single centre, randomised, double-blind phase 2 study.
Lancet Microbe 2024;5(7):645-654. - gov : https://clinicaltrials.gov/study/NCT072158588 (consulté le 03/03/2026)
- gov : https://clinicaltrials.gov/study/NCT03180801 (consulté le 03/03/2026)
- gov : https://clinicaltrials.gov/study/NCT04960397 (consulté le 03/03/2026)
- Eiden J, et al. M2-deficient single-replication influenza vaccine–induced immune responses associated with protection against human challenge with highly drifted H3N2 influenza strain. J Infect Dis 2022;226(1):83-90
- gov : https://clinicaltrials.gov/study/NCT06087640 (consulté le 03/03/2026)
- gov : https://clinicaltrials.gov/study/NCT02918006 (consulté le 03/03/2026)
- Nguyen TQ, et al. Animal models for influenza research: Strengths and weaknesses. Viruses 2021;13(6):1011.