Fièvres hémorragiques virales
Les fièvres hémorragiques virales (FHV) regroupent différentes maladies (Ebola, fièvre de Lassa, de Marburg, fièvre de Crimée-Congo...).
Dernière mise à jour le 06 novembre 2025
L’essentiel
- Les fièvres hémorragiques virales (FHV) regroupent différentes maladies (Ebola, fièvre de Lassa, de Marburg, de Crimée-Congo…) qui se manifestent par des symptômes communs : forte fièvre, douleurs musculaires et articulaires, hémorragies, diarrhée et vomissements…
- Ces maladies peuvent être graves (taux de létalité moyen de 1 % pour la fièvre de Lassa,1 de 50 % pour Ebola2,3 et la fièvre hémorragique de Marburg,4 et de 40 % pour la fièvre de Crimée-Congo.5
Origine des fièvres hémorragiques virales
Historique
La fièvre jaune est un exemple séculaire de fièvres hémorragiques virales (FHV).6 La Chine ancienne, la Mandchourie en 1930, des pays d’Europe du Nord-Ouest en 1934, la Corée dans les années 1950 ont connu, sous différents noms, une fièvre hémorragique virale aiguë d’allure épidémique, associée à une atteinte rénale aiguë.6 En 1962, Gajdusek regroupa ces infections manifestement proches sous le terme de fièvre hémorragique avec syndrome rénal (FHSR) à l’origine de laquelle on retrouve les virus d’un même genre (Hantavirus) appartenant à la famille des Bunyaviridae.6
Il est apparu en fait que les FHV forment un groupe de maladies virales hétérogènes impliquant différentes familles de virus.6,7 L’émergence et la réémergence des fièvres hémorragiques virales est une préoccupation mondiale croissante.8
Ces vingt dernières années, la Région de la Méditerranée orientale a connu des flambées majeures et des cas sporadiques de fièvre jaune, de fièvre de la vallée du Rift, de dengue sévère et de fièvre hémorragique de Crimée-Congo dans plus de 12 pays.8 L’épidémie d’Ebola, survenue en 2015 en Afrique de l’Ouest, a provoqué plus de 29 000 malades et environ 11 000 décès.9
La biologie des virus responsables des FHV, leur épidémiologie et leur létalité sont très variables : de 1 % pour la fièvre de Lassa,1 de 50 % pour Ebola2,3 et la fièvre hémorragique de Marburg,4 et de 40 % pour la fièvre de Crimée-Congo.5
La mobilisation sans précédent qui a suivi l’épidémie d’Ebola a mis en évidence le besoin de mettre en place des actions de recherche structurantes permettant de mieux se préparer aux épidémies de fièvres hémorragiques virales qui présentent des risques de santé publique en raison de leur potentiel épidémique et/ou de l’absence ou de l’insuffisance des contre-mesures.
Les virus
Différentes familles de virus sont impliquées dans le développement des FHV :6,7
- Les Flaviviridae dont les virus du genre Flavivirus provoquent fièvre jaune et dengue hémorragique
- Les Bunyaviridae comprenant les Hantavirus, les Phlebovirus, à l’origine de la fièvre de la vallée du Rift, et les Nairovirus provoquant la fièvre hémorragique de Crimée-Congo
- Les Arenaviridae dont les Arenavirus, avec le virus de la fièvre de Lassa, sont associés à la fièvre de Lassa
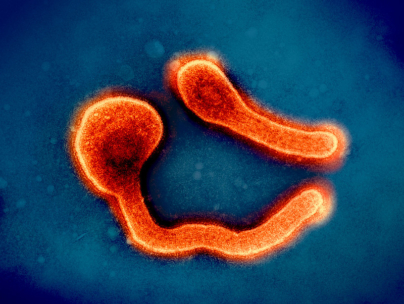
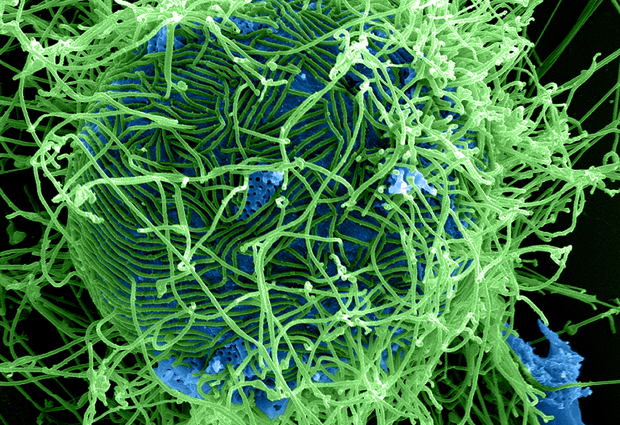
- Les Filoviridae dont le genre Filovirus comprend le virus Ebola et le virus de Marburg
Pour en savoir plus sur :
Gros plan sur les Filovirus
- Historique
Les Filovirus ont été découverts en 1967 lors de l’apparition d’un syndrome hémorragique sévère à Marbourg (Allemagne) et à Belgrade (Serbie).10 Le virus identifié a été nommé, à cette occasion, virus Marburg.10 En 1976, deux FEV survenaient, l’une au Soudan du Sud, l’autre en République démocratique du Congo. Il s’agissait de la première description, respectivement, du virus Soudan et du virus Ebola.10 Par la suite, à l’exception de quelques cas sporadiques, les Filovirus ne sont pas réapparus chez l’espèce humaine pendant 18 ans avant de ré-émerger sous formes de foyers épidémiques.10
En 2013, la maladie à virus Ebola apparaissait en Haute Guinée, se propageant au Liberia et en Sierra Leone, pour finalement constituer un foyer en Afrique de l’ouest et provoquer l’épidémie de Filovirus la plus dramatique à ce jour, avec plus de 29 000 malades et environ 11 000 décès entre décembre 2013 et juin 2016.9,10
Depuis, diverses maladies causées par un Filovirus ont été reportées, qu’il s’agisse de maladies à virus Marburg, de maladie Ebola à virus Ebola ou à virus Soudan.10
Jusqu’à présent, les épidémies causées par des Ebolavirus étaient circonscrites aux pays africains, mais ceci pourrait changer, des antécédents d’importation ayant été reportés en Europe et aux États-Unis.7,11
- Virus
Les Filovirus comprennent deux genres pathogènes pour l’homme : le genre Ebolavirus et le genre Marburgvirus.10 Le genre Ebolavirus comprend six espèces. Trois d’entre-elles sont hautement pathogènes pour l’humain : Zaïre ebolavirus (virus Ebola), Bundibugyo ebolavirus (virus Bundibugyo) et Sudan ebolavirus (virus Soudan).10
Les virions disposent d’une enveloppe et sont de morphologie variable. Le génome est une molécule d’ARN simple brin, de polarité négative codant sept protéines.10 Dans le cas des Ebolavirus, le gène viral code une protéine sécrétée par les cellules infectées, la sGP (glycoprotéine sécrétoire). La sGP se transforme en une glycoprotéine structurale qui joue un rôle important dans la virulence, même s’il existe d’autres facteurs de pathogénicité.10
Transmission
Les modes de transmission des FVH est multiple.8 La transmission peut se faire par contact avec des animaux porteurs (carcasses ou fluides d’animaux contaminés par exemple pour les fièvres de Lassa, Marburg ou Ebola), par piqûres d’insectes (moustiques, tiques pour les fièvres de Crimée-Congo et de la vallée du Rift) et par transmission interhumaine (sang, sécrétion, etc.).7,8 Dans l’immense majorité des cas la transmission d’une personne à l’autre s’effectue par contact direct avec des patients symptomatiques, avec du sang ou des liquides biologiques contaminés ; la fièvre de Lassa, elle, peut se transmettre par voie respiratoire.7,8
Le risque d’importation des virus responsables de FHV est différent selon le type de virus, le temps d’incubation et la rapidité d’installation des signes hémorragiques.7
Gros plan sur les Filovirus
Le cycle des Filovirus est réalisée dans des espèces animales réservoirs sauvages, peut-être des chauves-souris.10 Une transmission occasionnelle à l’être humain par transgression de la barrière des espèces est possible ; elle se fait par contact avec des tissus ou du sang d’animaux sauvages infectés, par contact direct ou indirect par manipulation d’un hôte accidentel.10 Les grands singes jouent souvent un rôle primordial dans la transmission du virus Ebola en tant qu’hôtes intermédiaires, dans la mesure où ils sont chassés comme viande de gibier.10
La transmission zoonotique du virus Marburg résulte souvent de contacts entre les chauves-souris frugivores égyptiennes, réservoir naturel du virus, et l’espèce humaine.10
La transmission interhumaine des Filovirus se fait principalement :10
- Par contact direct avec un patient symptomatique excréteur ou un cadavre
- Par contact avec des fluides biologiques et excrétas corporels infectés (sang, selles, vomissements, sperme, lait maternel)
- Avec des surfaces de l’environnement contaminées et imprégnées
La transmission du virus se fait par les mains, la muqueuse oculaire constituant une porte d’entrée opportune.10 La transmission sexuelle des hommes aux femmes est également possible pour les virus Ebola et Marburg.10,12 La transmission interhumaine peut-être accrue en milieu hospitalier (infection nosocomiale) par contact avec le sang virémique, déclenchant des explosions épidémiques meurtrières de fièvres Marburg ou Ebola.6,7
Symptômes
Le tableau clinique comporte, à des degrés divers, une fièvre, des signes hémorragiques et une défaillance circulatoire.7 On peut citer d’autres symptômes tels que :13
- Diarrhée
- Vomissements
- Fatigue
- Anorexie
- Céphalées
- Douleurs musculaires
- Douleurs articulaires
- Douleurs abdominales
- Douleur à la déglutition (odynophagie)
- Saignements inexpliqués
Les FHV se caractérisent en général par une évolution biphasique : la première phase de quelques jours est dominée par un syndrome pseudo-grippal sans spécificité ; la seconde phase hémorragique (hémorragies cutanées, suffusions hémorragiques*, hémorragies viscérales souvent fatales), diffuse et parfois impressionnante, évolue souvent rapidement et est fréquemment accompagnée d’un état de choc.7
*épanchement de sang en dehors du vaisseau qui le contient, en direction des tissus avoisinants
Diagnostic
Aux premiers stades d’une épidémie, il est difficile de distinguer une FHV d’autres infections courantes comme le paludisme, la fièvre typhoïde, d’autres infections bactériennes ou la gastroentérite aiguë.14
Par la suite, il est très difficile de distinguer entre-elles les différentes FHV ; cependant, il existe certaines particularités attachées à l’une ou l’autre des maladies. Ainsi, Ebola est caractérisée par une prédominance des signes digestifs, la fièvre de la Vallée du Rift par une atteinte ophtalmologique et la fièvre de Crimée-Congo par une rhabdomyolyse**.7
** destruction massive des cellules du tissu musculaire squelettique
La prise en charge
Le traitement du patient doit être instauré au plus tôt pour limiter toute perte de chance.13
Traitement symptomatique
Le traitement symptomatique doit être immédiat et adapté aux signes de gravité. Il comprend :13
- Des mesures d’hydratation et de rééquilibration hydro-électrolytique, antiémétiques, anti-diarrhéiques, antipyrétiques et antalgiques
- Des mesures de réanimation si nécessaire
Les anti-inflammatoires non stéroïdiens (AINS) et les anticoagulants sont contre-indiqués.
Traitement anti-infectieux probabiliste
La prise en charge du choc septique chez l’enfant, l’adulte et l’adolescent comprend l’utilisation d’une antibiothérapie et/ou un traitement antipaludique.13,14
Traitement spécifique
Il est nécessaire de distinguer le virus Ebola du virus de Lassa, puisque seul le virus de Lassa peut être traité par la ribavarine.14 En dehors de cette différence spécifique de traitement, la prise en charge clinique repose sur le traitement symptomatique pour Ebola, Marburg, la fièvre de Lassa et la fièvre hémorragique de Crimée-Congo.14
Dans le cas de la maladie à virus Ebola causée par le virus Ebola Zaïre, une combinaison de trois anticorps monoclonaux (atoltivimab/maftivimab, odesivimab ; Inmazeb) et un anticorps monoclonal (ansuvimab ; Ebanga) peuvent être prescrits chez l’adulte et l’enfant.13
Actions de recherche de l’ANRS Maladies infectieuses émergentes sur les fièvres hémorragiques virales et les filovirus
Direction du CORC sur les filovirus
Début 2025, l’ANRS MIE a été désignée pour diriger le Consortium de recherche ouverte collaborative (CORC) sur les filovirus et est en passe de devenir un centre collaborateur de l’OMS.
Les CORC sont des réseaux internationaux d’institutions de recherche dont la mission est de renforcer la préparation mondiale aux pandémies grâce à la recherche collaborative, le partage des connaissances et le développement rapide de contre-mesures. Une première réunion, tenue le 13 février 2025, a été consacrée aux essais thérapeutiques et aux recherches prioritaires sur les contre-mesures médicales. Dans le cadre du CORC, des priorités de recherche ont été définies par l’ANRS MIE et l’OMS, et un travail est en cours avec l’ensemble des experts du « CORC filovirus » pour mettre à jour les priorités et retards en terme de recherche définis par la feuille de route du consortium MARVAC.
Activation d’une cellule Emergence
En mars 2025, le pôle « Veille et Réponse aux épidémies » de l’ANRS MIE a activé une cellule Emergence de niveau 1 sur les filovirus. Cette cellule pérenne comprend une veille scientifique dont les premières éditions porteront sur le virus Marburg circulant actuellement en Tanzanie et sur le virus Ebola Soudan à l’origine d’une épidémie en cours actuellement en Ouganda.
Action coordonnée sur les fièvres hémorragiques virales
En 2024, l’ANRS MIE a mis en place une action coordonnée sur les fièvres hémorragiques virales présidée par Sylvain Baize, Marie Jaspard et Abdoulaye Touré. Ce groupe d’échange et de réflexion stratégique est consacré notamment à la recherche scientifique sur les filovirus et a pour objectif, à travers ces groupes de travail (thérapeutique, faune sauvage, vaccins), de faire émerger des projets de recherche dans le cadre de collaborations internationales, principalement avec nos partenaires en Afrique.
Références
- OMS : Fièvre de Lassa. https://www.who.int/fr/news-room/fact-sheets/detail/lassa-fever (consulté le 08/08/2025)
- Izudi J, Bajunirwe F. Case fatality rate for Ebola disease, 1976–2022: A meta-analysis of global data. J Infect Public Health 2024;17:25–34
- OMS : Ebola (maladie à virus). https://www.who.int/fr/news-room/fact-sheets/detail/ebola-disease (consulté le 08/08/2025)
- OMS : Maladie à virus Marburg. https://www.who.int/fr/news-room/fact-sheets/detail/marburg-virus-disease (consulté le 08/08/2025)
- OMS : Fièvre hémorragique de Crimée-Congo. https://www.who.int/fr/news-room/fact-sheets/detail/crimean-congo-haemorrhagic-fever (consulté le 08/08/2025)
- Vachon F. Fièvres hémorragiques virales. 1ère partie : Maladies historiques, maladies nouvelles émergentes. Réan Urg 1998 ; 7 : 389-402
- Tattevin P, et al. Les fièvres hémorragiques virales. Rev Francoph Lab 2026 ; 480 : 71-80
- OMS : Fièvres hémorragiques virales. https://www.emro.who.int/fr/health-topics/haemorrhagic-fevers-viral/introduction.html (consulté le 08/08/2025)
- OMS : Fin de la flambée d’Ebola la plus récente au Libéria; des résurgences pourraient se produire. https://www.who.int/fr/news/item/14-01-2016-latest-ebola-outbreak-over-in-liberia-west-africa-is-at-zero-but-new-flare-ups-are-likely-to-occur (consulté le 08/08/2025)
- Malvy D. Ebola et la maladie à filovirus : enjeux et perspectives à l’horizon 2030. Bull Acad Natl Med 2023 ; 207 : 787—805
- Kerper M, Puckett Y. Filovirus. Continuing education activity. https://www.ncbi.nlm.nih.gov/sites/books/NBK544258/ (consulté le 08/08/2025)
- Subissi L, et al. Ebola virus transmission caused by persistently infected survivors of the 2014–2016 outbreak in West Africa. J Infect Dis 2018;218(suppl 5):S287-S291
- Avis portant sur la conduite à tenir face à des patients suspects de fièvre hémorragique virale (FHV) dont la maladie à virus Ebola (MVE). Haut Conseil de la santé publique, 20 octobre 2021. https://www.hcsp.fr/explore.cgi/avisrapportsdomaine?clefr=1129 (consulté le 08/08/2025)
- Prise en charge clinique des cas de fièvre hémorragique virale : guide de poche pour l’agent de santé de première ligne 2016 : guide d’urgence provisoire à adapter aux conditions d’exercice dans les différents pays. Organisation mondiale de la Santé, 2016. https://iris.who.int/bitstream/handle/10665/272720/9789242549607-fre.pdf?sequence=1&isAllowed=y (consulté le 08/08/2025)
L’actualité de l’ANRS MIE sur les fièvres hémorragiques virales

PEPR MIE – Publication du livret des lauréats 2023-2025 et chaires junior
Portrait des 34 projets de recherche et chaires junior financés par le PEPR MIE de France 2030.
02 mars 2026
Publications
- Kieh M. et al. Randomized Trial of Vaccines for Zaire Ebola Virus Disease. N Engl J Med. 2022.
- Diallo MSK, et al. Temporal evolution of the humoral antibody response after Ebola virus disease in Guinea: a 60-month observational prospective cohort study. The Lancet Microbe. 2021.
- Diallo MKS, et al. Understanding Long-term Evolution and Predictors of Sequelae of Ebola Virus Disease Survivors in Guinea: A 48-Month Prospective, Longitudinal Cohort Study (PostEboGui), Clinical Infectious Diseases. 2021.
- Keita, A.K., et al. Resurgence of Ebola virus in 2021 in Guinea suggests a new paradigm for outbreaks. Nature 2021.
- Cases of Crimean–Congo haemorrhagic fever in the EU/EEA, 2013–present